SCADA


医薬品製造におけるデータインテグリティ(DI)対応は各国の規制当局や国際基準に基づく義務です。
主な規定として、海外ではFDAの21 CFR Part 11やEUのGMPガイドライン、国内では日本のGMPガイドラインに基づき、
製造データや品質管理データの完全性・改ざん防止のための具体的な要件を設けています。
これらの要件に対して人手による対応は可能ですが限界があり、規制遵守の観点からもリスクが高いです。
日阪製作所では「HIDIAS™」を使用することでDI対応をより確実に効率的に行うとともに、
製造管理にも活かせるシステムを提案します。
特長
 日阪製作所独自のサービス
日阪製作所独自のサービス
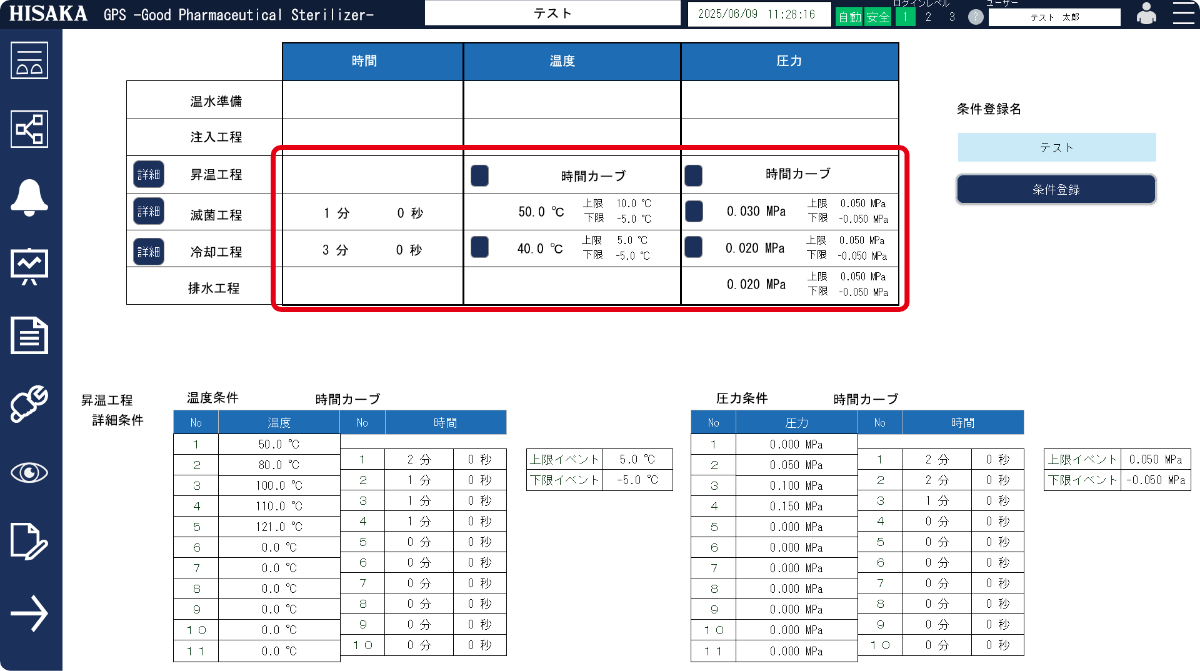
レシピ管理
パラメーター管理
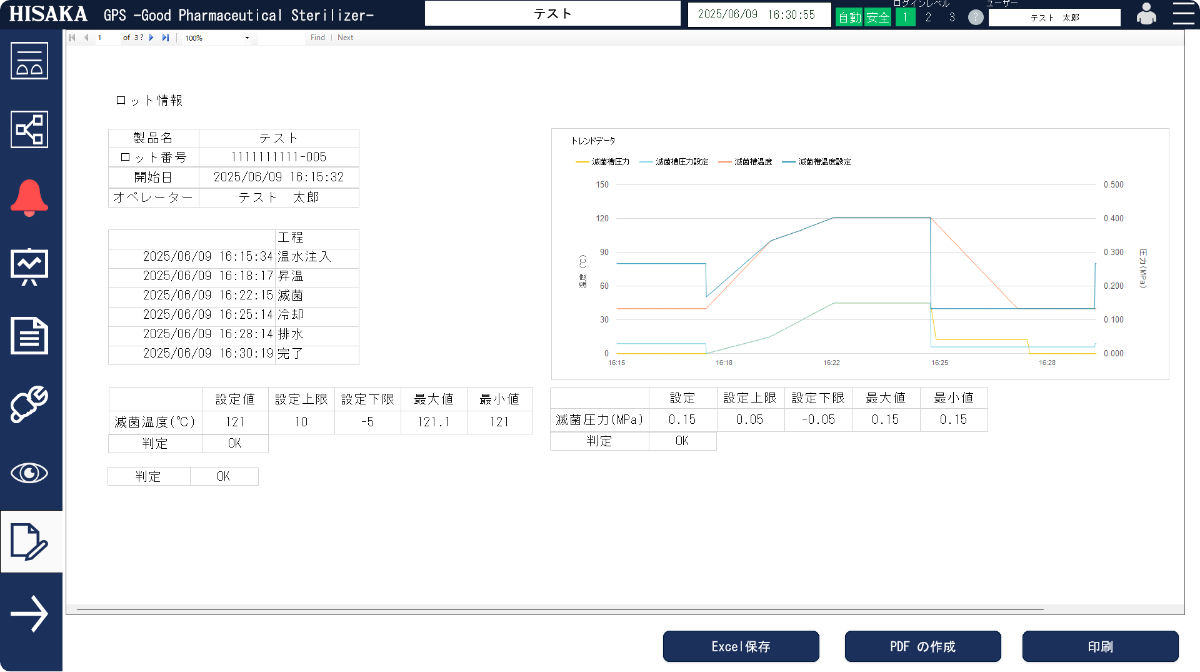
レポート機能
システム構築
リソース削減
 SCADAシステムを導入するメリット
SCADAシステムを導入するメリット
ペーパーレス化
省人化
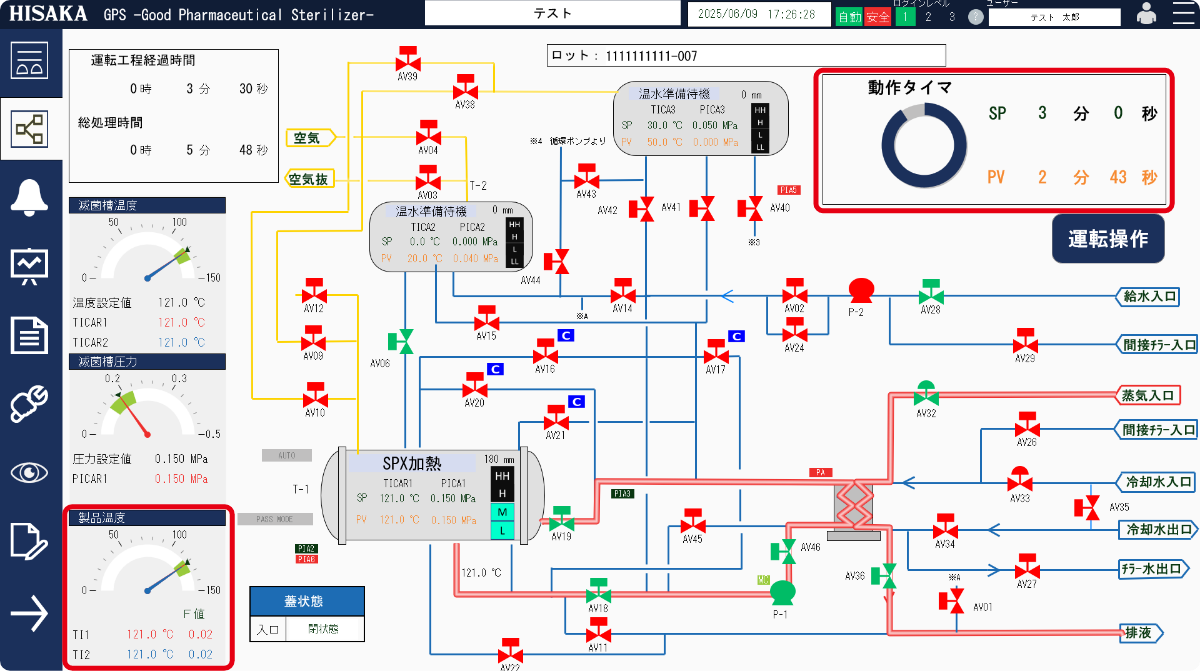
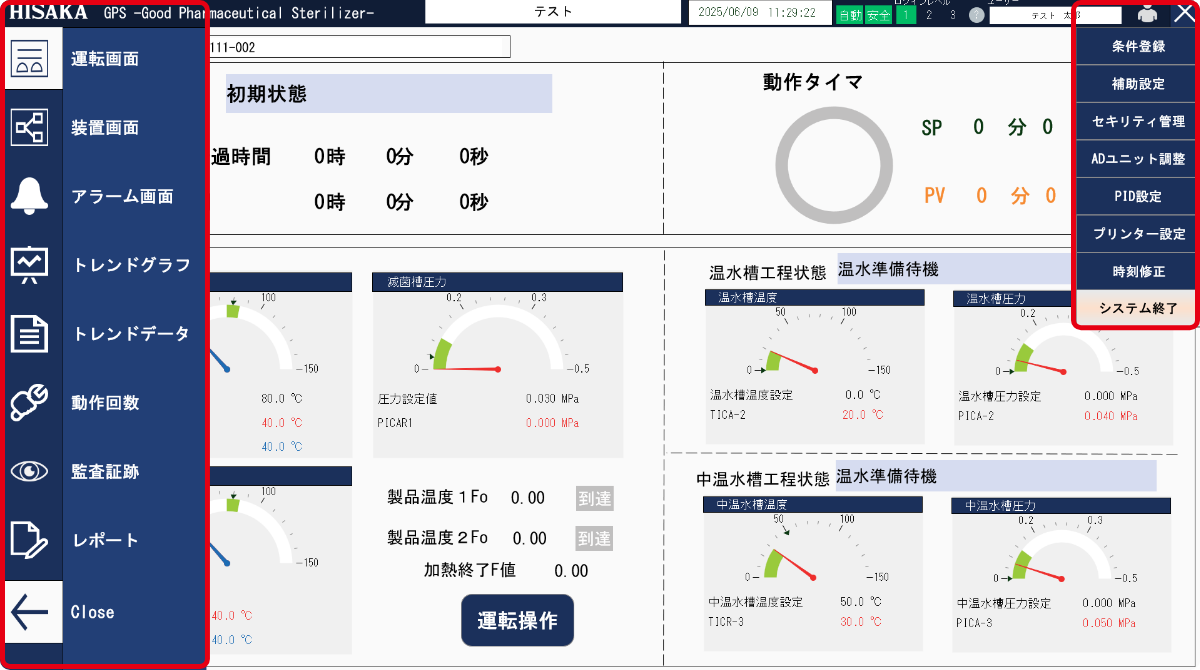
監視・制御・管理
設備の効率化DI対策
セキュリティの
厳格化
SCADAの新機能
- 01記録計+タッチパネルの
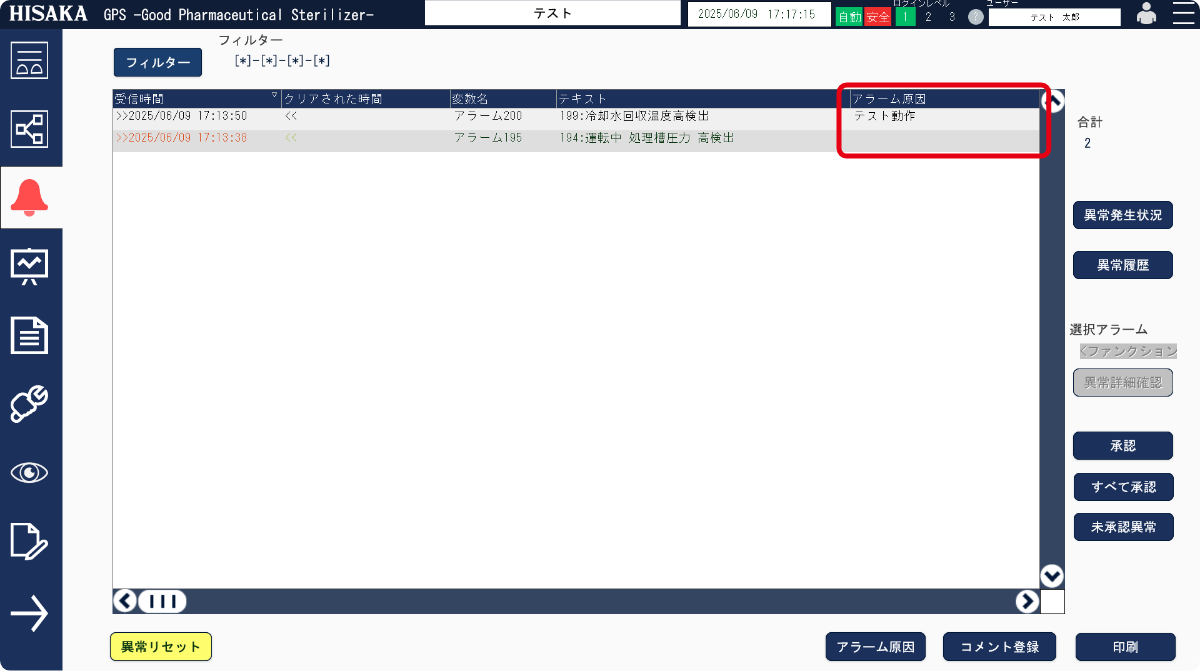
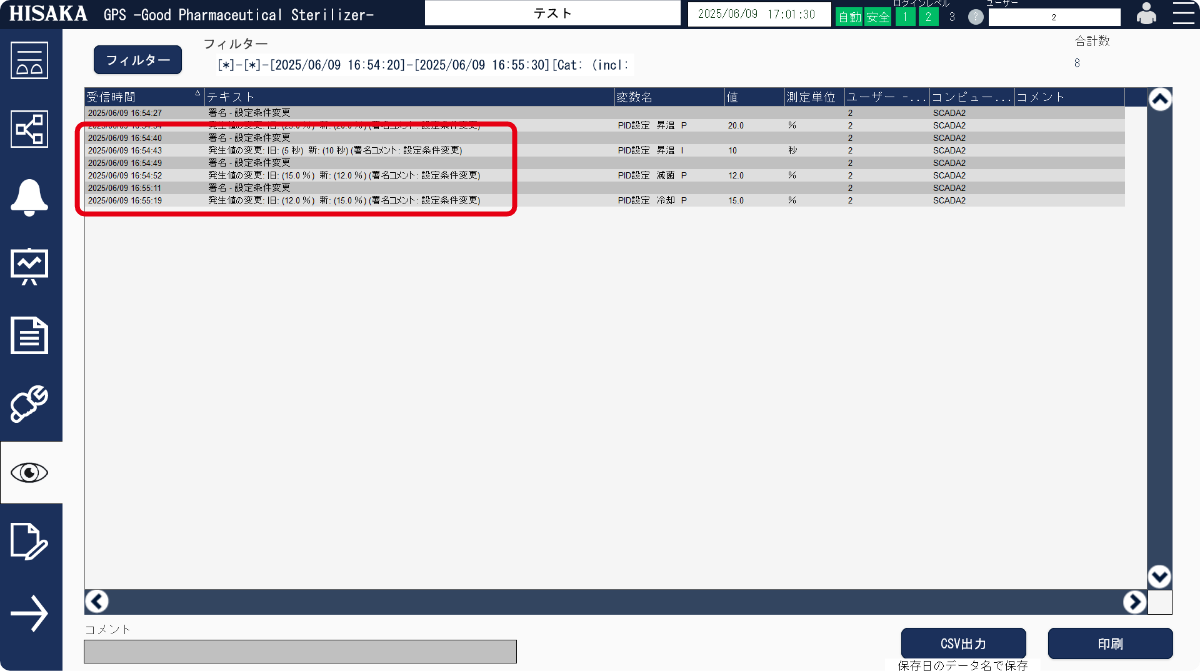
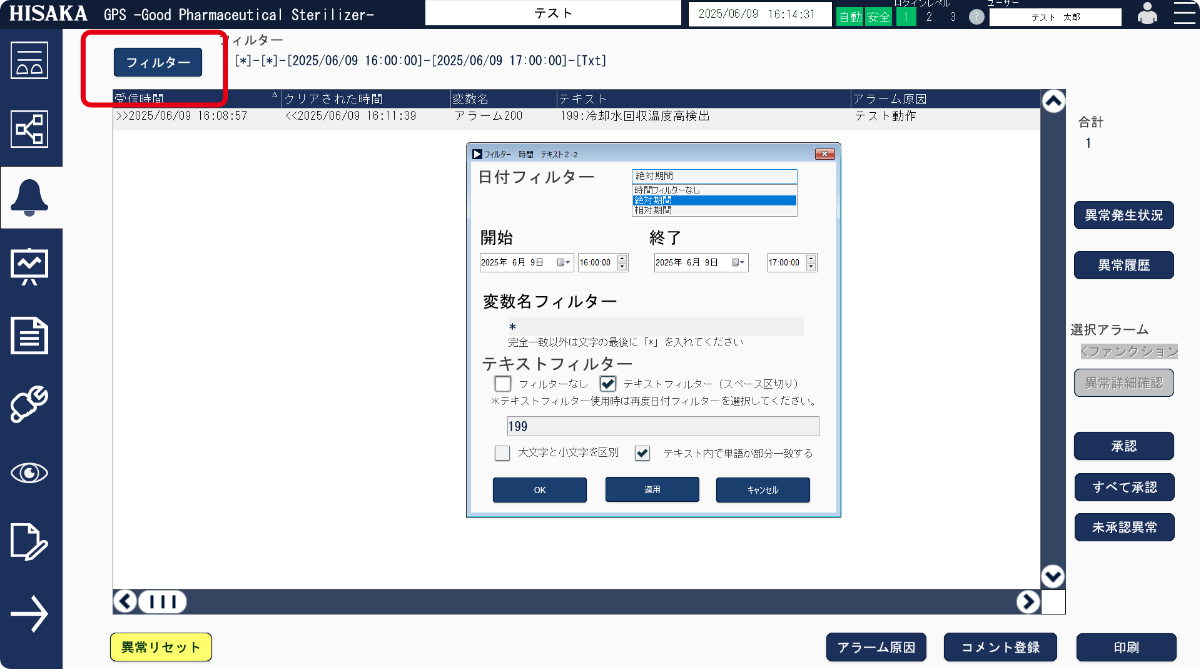
機能をSCADAへ集約 - 02DI対応で監査証跡を簡単管理
検索も可能 - 03レシピ管理が可能
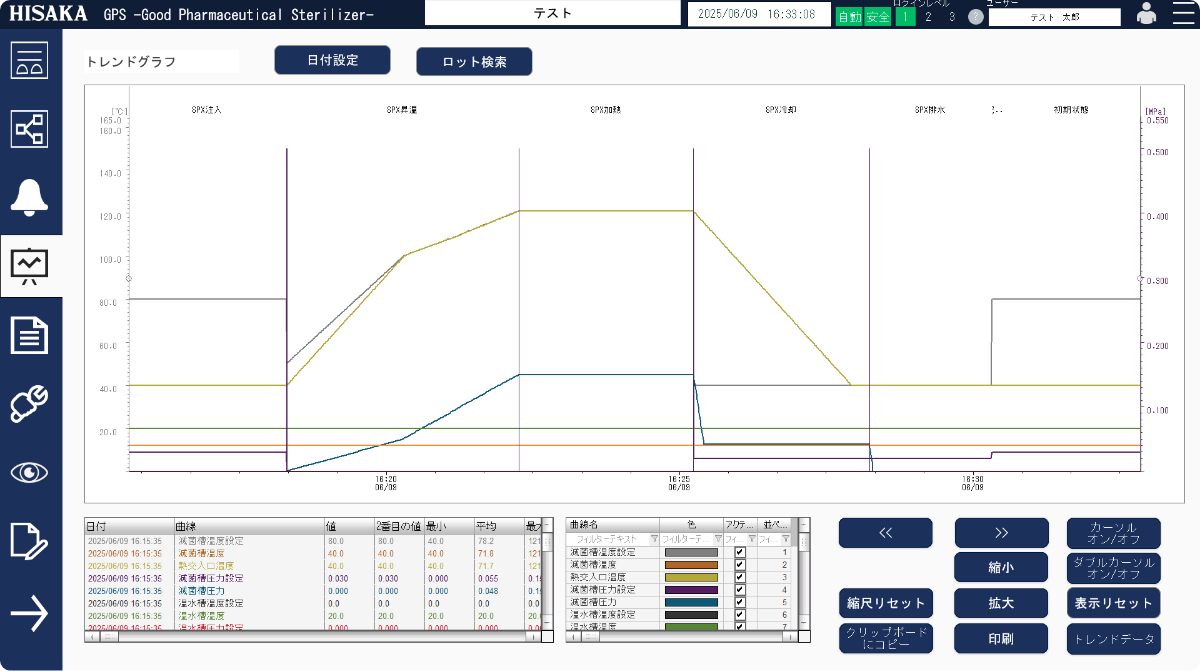
- 04直感的なグラフィック表示
製造管理・監視システム
「HIDIAS™」の導入により
リソース削減
- 重要ポイントを熟知しているメーカーが過剰設計を防止し、必要機能を完全網羅
- 日阪製作所の装置から始めるスモールスタートでシステム導入リスクを低減
- 検証済ソフトによりGMP/CSV対応の負担を軽減
- メーカー独自の最適化仕様で、SCADAの操作性・信頼性向上
誰でも分かりやすい、
使いやすいシステム
設備のリアルタイム監視、異常・逸脱時の対応と証跡を残し、
製造現場のトレーサビリティと透明性を強化します。
 作業者目線
作業者目線
 管理者目線
管理者目線
用途
監査証跡、DI(データインテグリティ:データ整合性)対策





